精确筛查风险分层—HPV与子 宫颈癌 防治
北京协和医院妇产科主任 郎景和
宫颈癌 是中国女性第二大最常见的恶性 肿瘤 。据世界卫生组织估计,全世界每年有逾 47 万新发 宫颈癌 病例,中国每年新发 宫颈癌 病例数约占世界总发病数的 28% 。 南方医科大学南方医院妇产科张广亮
由于几乎所有的 宫颈癌 的病例样本中都能找到人乳头瘤病毒( HPV ),从而印证了 HPV 是 宫颈癌 的致病病毒,也使得 宫颈癌 成为目前人类所有癌症病变中唯一病因明确的癌症。 HPV 感染 是一种很常见的 感染 ,高达 75% 的女性在其一生中可能 感染 HPV ,在 30 岁以下( 18 - 28 岁)性活跃的年轻女性中亦不鲜见( 4-15% ),且终身积累的概率高达 40% ,但这种 感染 通常是“一过性”的或者称为“一过性 HPV 携带状态”,平均 感染 时间为 8 个月,多数可以清除,并不会发展为癌前病变。而 30 岁以上妇女 HPV 持续 感染 平均 8-24 个月可发生 宫颈癌 前病变( 宫颈上皮内瘤变 CIN ),平均 8-12 年可发展为浸润癌。因此, 高危型 HPV 持续性的 感染 是宫颈 癌前病变和 宫颈癌 发生的元凶。
高风险 HPV 检测联合细胞学:更精确的 宫颈癌 筛查手段
美国癌症学会( ACS )、美国阴道镜检查与宫颈病理学会( ASCCP )和美国临床病理学会( ASCP )认为: 宫颈癌 筛查最佳策略应当最大化筛查的益处、最小化筛查的潜在危害。 对于 HPV 检测来说,最重要的检测指标是灵敏度和阴性预测值 , 来决定哪些人可以回到常规人群管理,而不需要进一步的治疗。 因此, HPV 筛查的目的是发现真正有高风险人群,而非检测单纯的 HPV 感染 者。
2012 年美国预防服务工作组( USPSTF )发布的新版 宫颈癌 筛查指南以及 ACS 、 ASCCP 、 ASCP 联合发布的 2012 年新版 宫颈癌 筛查指南中,对于 30 — 65 岁的女性,优先推荐每 5 年进行细胞学和高危型 HPV 联合检测。若高危型 HPV 检测为阴性,则 5 年内无需再接受筛查;若细胞学检测为阴性,高危型 HPV 检测为阳性,则需要每年重复进行联合检测。
HPV16/18 分型:有助于更好的对 宫颈癌 高风险人群进行风险分层管理
事实上,采用 HPV 检测进行筛查给临床会带来一些新的困惑和质疑,比如,细胞学阴性、 HPV 阳性的状况可否被视为“新的 ASCUS ”?临床上该如何进行后续的管理?欧洲生殖道 感染 和 肿瘤 研究组织( EUROGIN )在 2008 年提出的 宫颈癌 防治策略中,设想通过 HPV16/18 基因分型、 p16 或其它生物标记物,对细胞学阴性、 HPV 阳性的人群进行分流,早期发现高风险人群。
一项美国最大型的 宫颈癌 筛查临床研究( 47,208 名女性参与、持续 5 年) ——ATHENA 研究发现 :细胞学漏诊的高度宫颈上皮内瘤病变中,有 1/3 为 HPV16 和 / 或 HPV18 阳性。 细胞学阴性但 HPV16 阳性的女性,发生 CIN2 以上病变的风险为 13.6% ,亦即平均每 8 个人中就有 1 人被细胞学漏诊的 CIN2 及更高级别病变。细胞学阴性但 HPV18 为阳性的女性,发生 CIN2 以上病变的风险为 7% 。细胞学 ASC-US 、高风险 HPV 群组阳性者发生 CIN2 及更高级别病变的风险,与 HPV16 和 / 或 18 阳性但细胞学阴性者的风险相当,应该立即进行阴道镜检查。所以,在筛查中结合 HPV16/18 基因分型,可以更好的对风险进行分层管理。
2013 年 ASCCP 新版指南也特别提出要对 细胞学阴性、 HPV 阳性的 30 岁以上女性进行 HPV16/18 基因分型检测(见下图),以及时发现细胞学正常结果中存在 CIN 的高危人群,以及意义未明的不典型鳞状细胞( AS-CUS )中需要更密切随访的人群。
30 岁以上,细胞学阴性、 HPV 阳性的女性如何进行管理
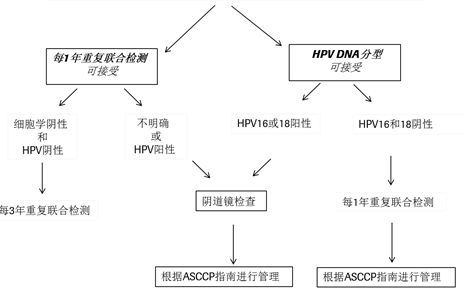
HPV DNA 检测: 有效分流 ASCUS 与 LSIL
ASCUS 是临床医生和细胞学技术人员及受检者遇到的最大困惑。其 数量大且去向不明,较难确认是正常,抑或已经出现 CIN 。在美国, ASCUS 和 LSIL 的发生率达 1.6—7.7 % ,其中 15%—30% 是 CIN 2/CIN 3 。可见 ASCUS 和 LSIL 也是一个不容忽视的问题,对于 ASCUS 和 LSIL 进行分流非常必要。
针对 ASCUS 和 LSIL 的分流检测,目前有三种常用方法: 1 、直接阴道镜检 联合 活检。这种方法不仅加重费用,还会对身体产生创伤,不适合大范围推广; 2 、重复细胞学追踪,受检者需要在第 12 、 18 、 24 个月时进行多次活检,但对于大多数可能正常的患者,复查细胞学会耗费很多时间,加重经济和精神负担; 3 、 HPV DNA 检测是被公认为最有效的检测方法。较之阴性患者, HPV 阳性患者发生 CIN1 的机会高 3.8 倍,发生 CIN2 和 CIN3 的机会高 12.7 倍。 HPV 阳性能预测不同级别 CIN 的发生,早期发现重度鳞状上皮内病变( HSIL ), 减轻病人焦虑 , 降低重复检查的花费。
HPV DNA 检测:指导 CIN 处理、治疗及术后随诊
作为 宫颈癌 及其癌前病变 CIN 的主要病因, HPV 的持续 感染 率和宫颈病变程度呈正相关。对 CIN 1 、 CIN 2 、 CIN 3 患者 中, 处理的方式不尽相同。临床上对于 CIN1 患者基本认为可以不予治疗,还存在着困惑和争议。 CIN1 的逆转、持续及进展分别为 60% 、 30% 及 10% 。由于进展很慢,发展为浸润癌的机会很小 ( < 1%) ,很可能导致过度治疗,从卫生经济学上也是不必要的。诚然, CIN1 的确有发展为 HSIL 和 宫颈癌 的潜在危险,通过 HPV DNA 检测可以帮助确定高风险的患者。而 CIN2 是 CIN1 到 CIN3 的过渡状态, HPV 阳性与 HPV 阴性会使 CIN2 的转归有很大区别,对临床决策有重要的参考价值。
此外, HPV DNA 检测在 CIN 患者的治疗及术后随诊中也起着重要作用。尽管对于 CIN 合理的、成功的治疗率可达到 90%—95% ,但经过治疗之后,复发率仍有 10% 。这些 CIN 患者未来 8 年内发展为 宫颈癌 的机会是普通人的 4 - 5 倍,其最大的危险来自治疗不当(残留)或是多灶性疾病复发。但切缘是否“干净”也并不是预测的良好指标,切缘“干净”者也可能出现残留和复发,所以患者需要继续随诊的同时还要检测 HPV 。常规要求 CIN 治疗后 4—6 个月进行第一次复查, 6—12 个月后再进行随访和检查。
根据 2012 年 ASCCP/ACS/ASCP 的报告:对于 HPV 检测方法的评估,应以 CIN2 和 CIN3 作为研究判定终点。 HPV 检测 CIN2+ 和 CIN3+ 的敏感度应该≥ 90% ,并建议不要将未经临床验证的 HPV 检测用于 宫颈癌 筛查。如果说 HC2( Hybrid Capture ) 开始了一场 HPV 检测及提高妇女健康和防治 宫颈癌 的革命,那么新方法 cobas 4800 HPV DNA 检测,则是推动了 宫颈癌 筛查技术的新进展,可同时提供 HPV16 、 18 分型结果和其他 12 个高风险 HPV 亚型汇总的结果,并具备经临床验证的判定标准( cut-off 值)和全自动化检测平台,在大样本筛查中具有独特优势,临床表现和重复性也符合当前对 HPV 检测的要求。该检测已获得美国 FDA 、欧盟 CE 认证和中国 SFDA 批准,在 宫颈癌 筛查及诊疗领域将拥有广阔的应用前景。























 打开APP
打开APP